作者:孙千 本文转载自公众号:老千和他的朋友们。原文地址:https://mp.weixin.qq.com/s/KRs0gJBRGzhGUEA0kO9t5w
1950 年至 1980 年是透射电子显微镜(TEM)的黄金时代,这一时期诞生了大量关于细胞结构的新发现,随后相关的生化研究与功能研究也相继展开。彼时,透射电子显微镜占据核心地位 —— 每一张新研究对象的显微照片都能带来全新信息,助力人们深入洞察细胞与组织的构成及其功能。
那个时代的杰出显微镜学家(包括帕拉德、波特、福西特、肖斯特伦、罗丁等众多学者),将细胞与组织图像的数据质量提升到了极高水平。如今,我们在顶级期刊上看到的图像,大多无法达到那一黄金时代的技术高度,在细节关注度、信息量以及纯粹的美感上也相形见绌。
由于尔根・罗斯(Jürgen Roth)和玛吉特・帕维尔卡(Margit Pavelka)编写的这部图谱却是一个重大例外:书中呈现的电子显微照片,其图像质量与信息量未打折扣且无与伦比,制作过程中尽显严谨与对细节的极致追求。图谱展示了各类特化细胞(如外分泌胰腺细胞、肠上皮细胞、神经元等)的丰富多样性,提醒读者:尽管每个细胞都具备常见的细胞器组合,但它们的组织方式却各具特色、辨识度极高,训练有素的研究者一眼便能区分。
这些信息对于当前的研究至关重要 —— 如今的研究重点是整合蛋白质组学、分子生物学、分子成像、生理学及病理学等多领域方法,以理解细胞功能及疾病中的异常机制。在当下这个时代,越来越多的研究者倾向于用现代光学显微镜技术替代电子显微镜,只因前者技术要求更低、更易获取。但这部图谱提醒我们:电子显微镜所获取的信息无价且不可替代,其带来的认知提升,与两种技术之间 1000 倍的分辨率差距(电子显微镜分辨率更高)相得益彰。事实上,图谱也让我们明白,这两种技术是互补关系,而非相互替代。
仔细研读书中的图像便会发现,即便是正常细胞的结构,也蕴含着许多尚未被发掘的细节 —— 对于愿意付出努力的研究者而言,这仍是一座有待探索的宝藏。尤其是在细胞病理学领域,相关研究才刚刚起步。
我们有理由期待,这部图谱将激发读者开展更多关于正常及病变细胞的超微结构研究与功能研究,从而收获更为详尽的洞察。在基因组学与蛋白质组学蓬勃发展的今天,我们同样不应忘记关注 “结构组学” 的探索 —— 这部图谱正是读者开启这一探索之旅的绝佳起点。
M. G. Farquhar
参考资料Functional Ultrastructure Atlas of Tissue Biology and Pathology
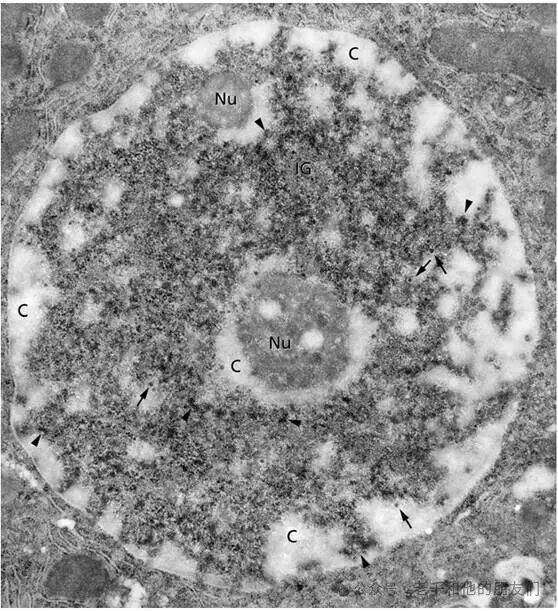
图 1 核糖核蛋白(RNP)的细胞化学检测(退行性 RNA 对比染色法)
样本为戊二醛固定的大鼠肝脏环氧树脂超薄切片,采用 Bernhard 退行性对比染色法:先以醋酸铀染色 DNA 和 RNA,再用 EDTA 水溶液孵育使铀离子从 DNA 脱离,最终让含 RNP 的核组分优先显色(需酶解对照实验验证染色特异性)。
图中可清晰分辨:箭头标记的染色质周围纤维(常规染色难区分)及染色质周围颗粒(推测为前体 mRNA 的核内储存 / 运输形式),染色质间颗粒(IG)、核仁(Nu);含 DNA 的外周染色质和核仁相关浓缩染色质(C)呈浅灰色。放大倍数:×24,500
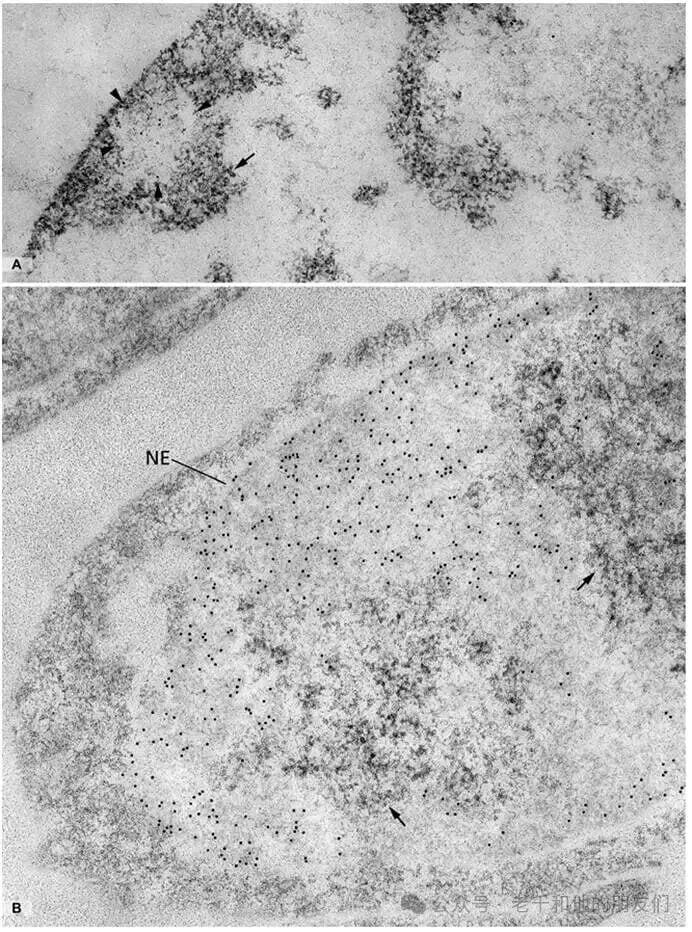
图 2 DNA 复制位点与间期染色体结构域检测(免疫电子显微镜)
样本为 V79 仓鼠细胞,通过掺入胸腺嘧啶类似物 BrdU 标记 DNA,再用单克隆抗 BrdU 抗体 + 金标记二抗检测,部分样本结合饿酸胺 Feulgen 型反应显色。
A 图:BrdU 孵育 2 分钟,金颗粒(新生 DNA 位点)主要分布于浓缩染色质区域外围的分散染色质纤维(箭头),该区域含 DNA 聚合酶 α,提示 DNA 复制位点集中在染色质周围区域,新复制 DNA 会向浓缩染色质内部移动;B 图:BrdU 孵育 9 小时后继续培养 62 小时(约 5 次细胞分裂),核内仅含 2-3 条标记染色体,可观察到染色体结构域(或被染色质间空间分隔,或紧密接触但 DNA 少混合),箭头指示染色质周围及染色质间区域的 RNP 纤维。标记:NE(核膜)。放大倍数:A 图 ×66,000;B 图 ×63,000
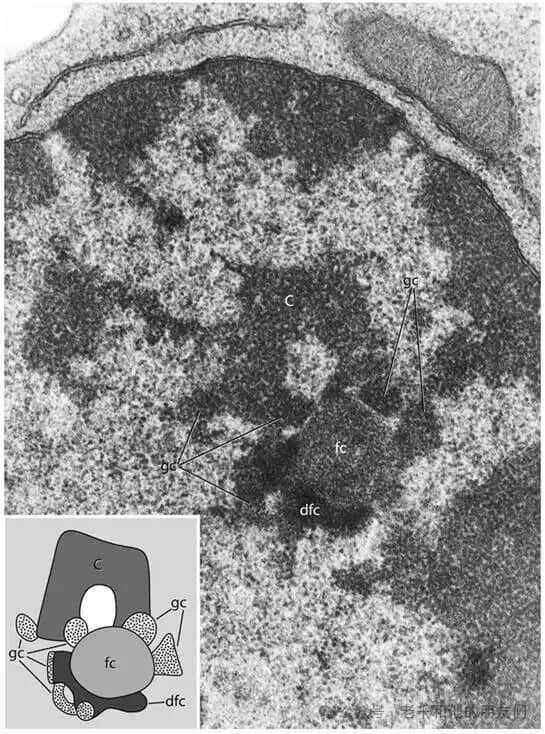
图 3 核仁的超微结构与功能关联
核仁是核内最显著结构,围绕核仁组织区(NOR,含大量 pre-rRNA 编码基因)形成,人类二倍体细胞理论可形成 10 个核仁,间期融合后通常含 1-4 个,核心功能为核糖体前体合成与组装,还兼具 tRNA 成熟、衰老调控等额外功能。
图中核仁由三部分组成:纤维中心(fc,蛋白质储存位点,球形)、致密纤维组分(dfc,含早期核糖体前体)、颗粒组分(gc,含接近成熟的核糖体前体),伴随大量浓缩染色质(C);转录位点存在两种假说(dfc 内或 fc 与 dfc 交界处,或 fc 为主要位点)。核仁与卡哈尔体(CB)关系密切,二者间存在蛋白质移动和物质转移(部分蛋白质共定位,CB 可向核仁移动并接触)。放大倍数:×66,000
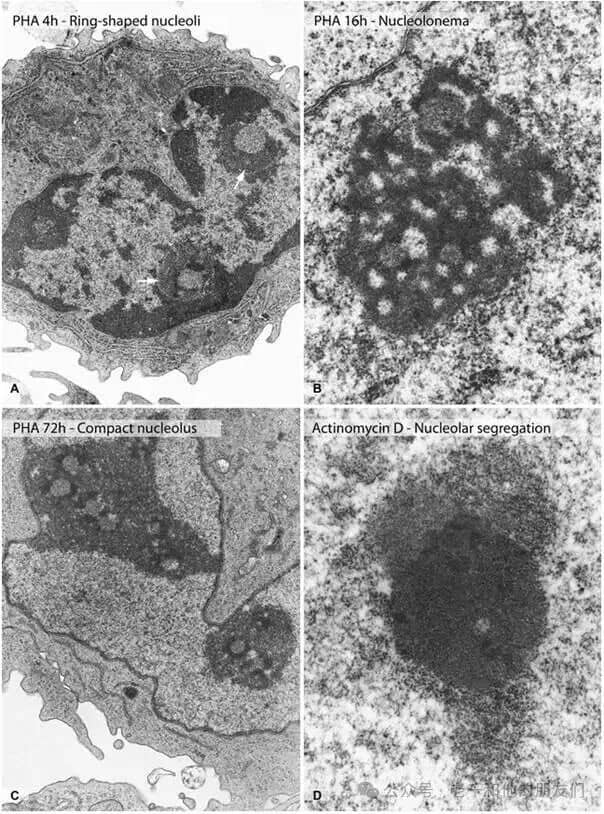
图 4 核仁结构的动态变化(PHA 刺激人类淋巴细胞)
核仁结构随细胞功能状态改变,以 PHA 刺激的人类淋巴细胞为模型,可分为三种类型:A 图(PHA 刺激 4 小时):环状核仁(箭头),含大纤维中心,周围环绕 dfc 和 gc,未受刺激的淋巴细胞 75% 为该类型;B 图(PHA 刺激 16 小时):核仁网型核仁,由 dfc 和 gc 构成扩展网络,纤维中心小而不明显(前期多个小核仁融合,蛋白质消耗导致),36 小时时最显著;C 图(PHA 刺激 72 小时):致密型核仁,含多个纤维中心,每个周围环绕厚层致密纤维物质,存在大面积颗粒状核仁物质,标志细胞进入高活性状态;D 图:放线菌素 D 处理 6 小时的 HeLa 细胞,rRNA 转录受抑制,核仁总体积缩小,fc、dfc、gc 相互分离,伴随大量浓缩染色质(C)。放大倍数:A 图 ×7,000;B 图 ×29,000;C 图 ×14,000;D 图 ×30,000
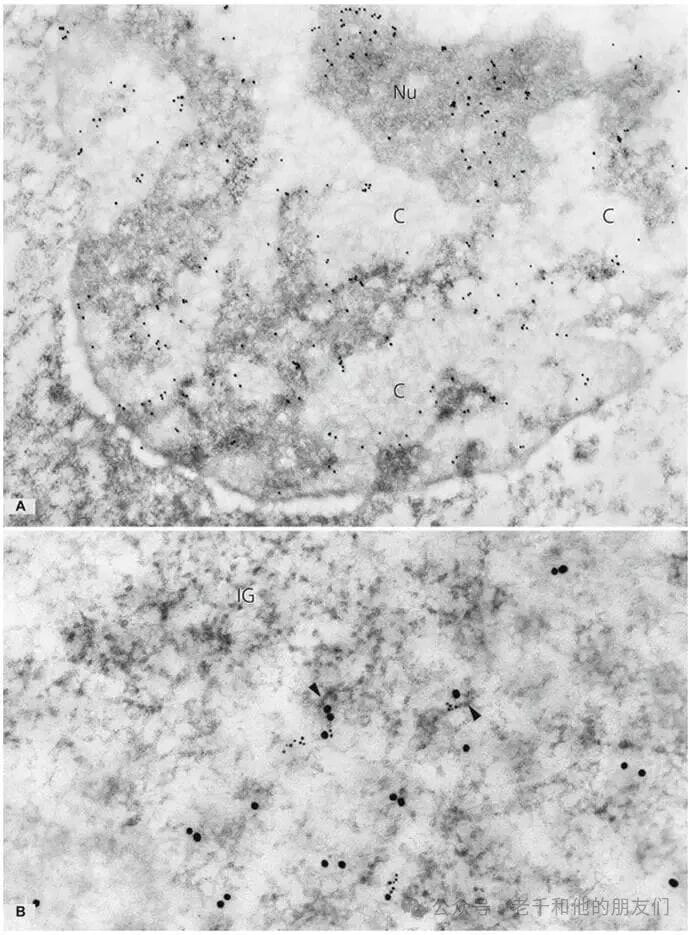
图 5 RNA 合成位点的免疫电子显微镜检测
采用免疫电子显微镜技术,以核苷酸类似物 BrUTP(或 BrU,需透化细胞、显微注射等处理)标记 RNA,结合单克隆抗溴脱氧尿苷抗体 + 金标记二抗检测,样本经甲醛 / 甲醛 – 戊二醛固定,包埋于环氧树脂或 Lowicryl K4M 等树脂以保证灵敏度。
A 图(人膀胱癌细胞系 T24,BrUTP 孵育 20 分钟):核质中免疫金标记集中在浓缩染色质(C)周边的染色质周围区域,核仁(Nu)内新合成 pre-rRNA 主要位于 dfc;B 图(BrUTP 孵育 10 分钟,双重免疫金标记):6nm 金颗粒(抗溴脱氧尿苷抗体,新转录 RNA)与 15nm 金颗粒(抗 hnRNP 核心蛋白抗体,hnRNP 复合物)共定位于染色质周围纤维(箭头,pre-mRNA 原位形式,推测为 pre-mRNA 加工场所),染色质间颗粒簇(IG,剪接因子聚集储存区)无标记。放大倍数:A 图 ×32,000;B 图 ×122,000
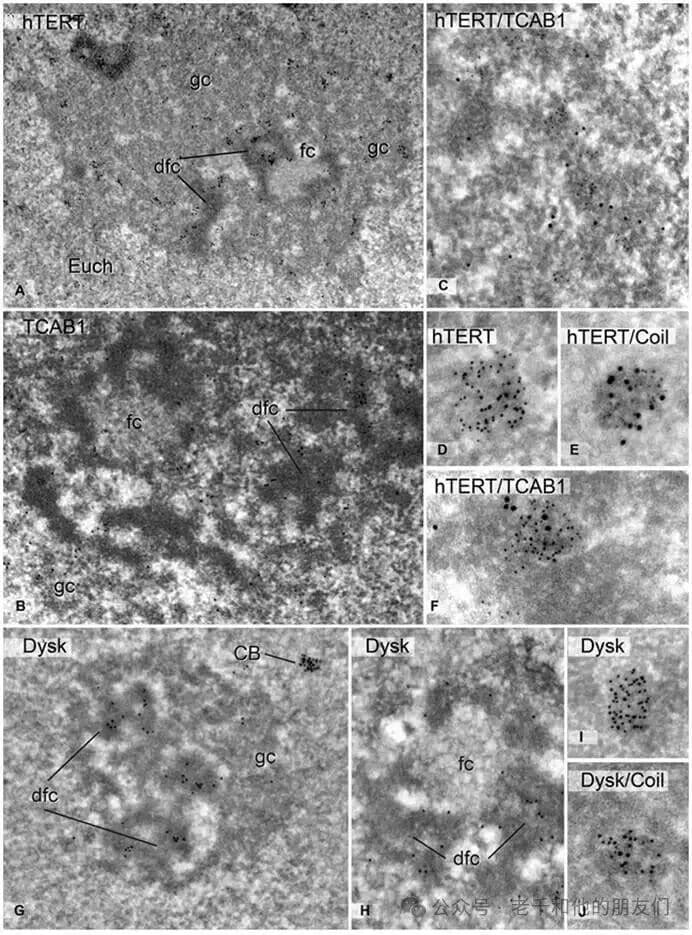
图 6 核仁、卡哈尔体与端粒酶组装
核仁(核糖体 RNA 合成及组装)与卡哈尔体(CB,核剪接机制组装 / 转录后修饰)功能关联,端粒酶(核糖核蛋白酶,含 TERT、TERC 等)的组装依赖二者相互作用。
S 期时:hTERT(A 图)和 TCAB1(B 图)定位于核仁 dfc 和 gc,且在 dfc 共定位(C 图,大金颗粒为 TCAB1,小金颗粒为 hTERT);hTERT(D 图)和 TCAB1(F 图)还存在于含线圈蛋白的 CB 中(E 图,大金颗粒为 hTERT,小金颗粒为线圈蛋白),CB 可位于常染色质(Euch)或与核仁结合;端粒酶必需组分 dyskerin(Dys)仅定位于核仁 dfc(G、H 图)和 CB(I、J 图,大金颗粒为 dyskerin,小金颗粒为线圈蛋白)。推测:端粒酶在核仁 dfc 组装并保留,结合 TCAB1 后运输至 CB,最终募集到端粒。标记:Euch(常染色质);fc(纤维中心)。放大倍数:A 图 ×4,500;B 图 ×9,000;C 图 ×22,500;D 图 ×8,000;E 图 ×20,000;F 图 ×23,000;G 图 ×9,500;H 图 ×8,000;I 图 ×13,000;J 图 ×15,000
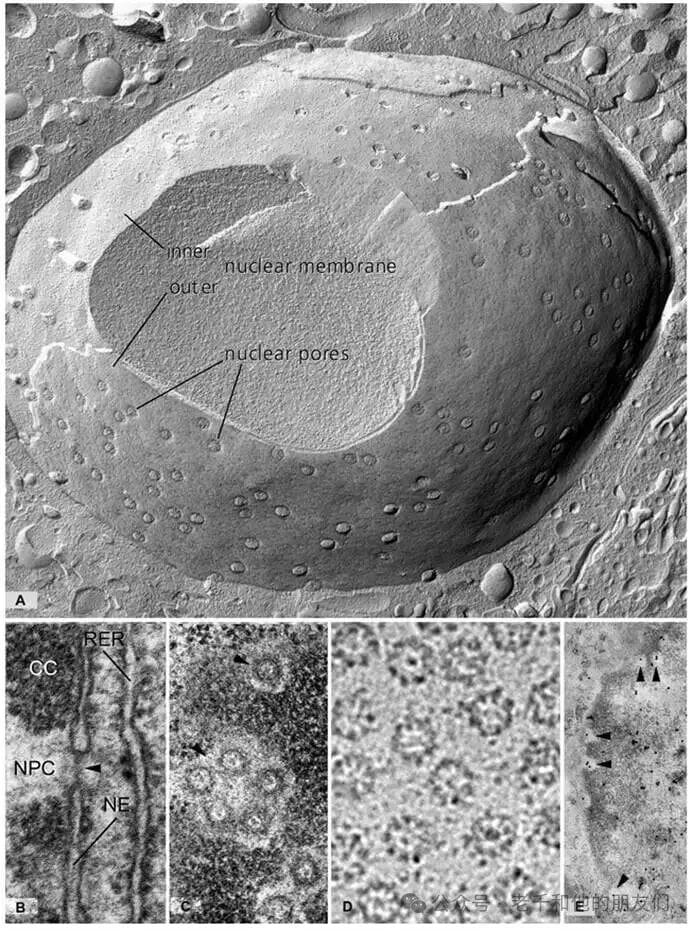
图 7 核孔复合体(NPC)的超微结构
核孔复合体是核膜上的大型大分子组装体(分子量约 1.25×10⁸道尔顿),每个核含 3000-4000 个,为双向运输通道。结构特征:圆柱形通道(直径约 125nm),由嵌入核膜的腔环、胞质侧环、核质侧环组成;8 个辐条构成桶状中央环(八重旋转对称性),辐条间形成 8 个纵向通道(直径约 10nm,小分子被动扩散),中央区域负责大分子主动运输(最大允许直径约 26nm,需受体蛋白);核质侧延伸 8 条长纤维,汇聚形成末端环(核篮结构)。
图中:A 图(冷冻断裂复制品):正面观察核外膜和核内膜上的大量 NPC;B 图(横截面):核内膜与核外膜在孔边缘相连,箭头示孔中央膜片样结构,核内膜表面有核纤层和浓缩染色质(CC),核膜(NE)旁细胞质含粗面内质网(RER);C 图(掠射切片):正面观察 NPC,孔中含电子致密颗粒,周围环绕环状外周颗粒物质(箭头),NPC 间为浓缩染色质(CC);D 图(冷冻电镜,去垢剂提取):端视视角下 NPC 由 8 个外周颗粒和 1 个中央颗粒构成;E 图(金标记):切向切片中 NPC 中心区域被金颗粒标记(箭头),示 O – 连接的 N – 乙酰葡糖胺残基(重要调控修饰)。放大倍数:A 图 ×30,000;B 图 ×42,000;C 图 ×36,000;D 图 ×121,000;E 图 ×17,000
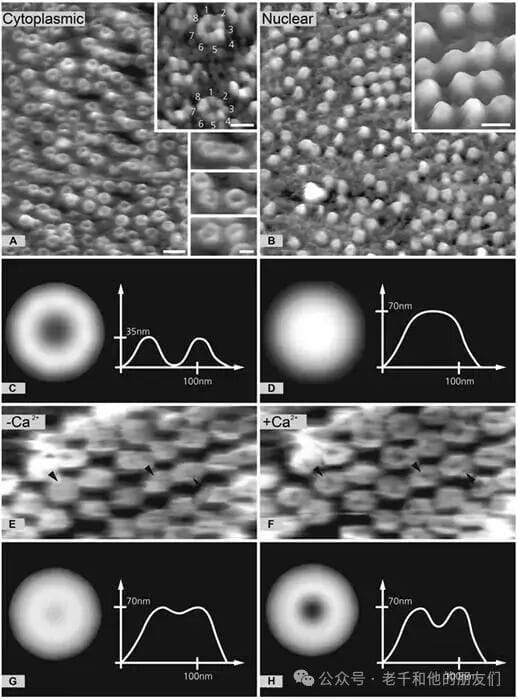
图 8 核孔复合体的钙调控动态变化(延时原子力显微镜)
采用原子力显微镜(AFM)在水溶液准生理条件下,观察非洲爪蟾卵母细胞核膜上天然 NPC 的静态结构与动态变化。
A 图(胞质面):NPC 呈 “甜甜圈” 状;B 图(核质面):NPC 呈 “圆顶” 状,二者均可见八重旋转对称性(A 图插图);C、D 图:对齐平均后的 NPC 径向高度分布。E 图(无钙条件):NPC 核质面呈关闭状态;F 图(微摩尔浓度钙条件):NPC 核质面呈开放状态,箭头标记的 3 个 NPC 显示该变化可逆;G、H 图:对齐平均后的径向高度定量分析,核篮远端环出现 20-30nm 直径开口,核篮整体高度不变,支持 “核篮及其远端环发挥虹膜式隔膜作用” 的假说(示意图示无钙时环关闭、有钙时环开放)。放大倍数:A、B 图 ×75,000;A、B 图上方插图 ×150,000;A 图下方插图 ×100,000;E、F 图 ×150,000
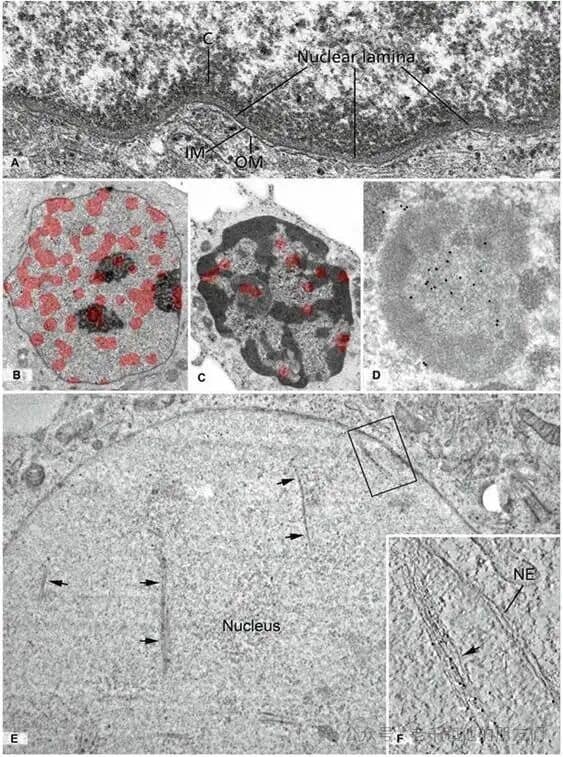
图 9 核骨架的核心成分(核纤层蛋白与肌动蛋白)
核骨架主要由核纤层蛋白和肌动蛋白(及结合蛋白)构成。
A 图(皮肤角质形成细胞):核内膜(IM)内侧的核纤层(30-80nm 纤维层),由核纤层蛋白 A/C 和 B(中间纤维类型)组成,锚定于核内膜,为核膜提供形态支持和机械稳定性,与染色质相互作用,有丝分裂时磷酸化解体、去磷酸化重组(突变可引发多种疾病);B 图(HeLa 细胞):免疫金标记显示肌动蛋白分布于常染色质;C 图(静息淋巴细胞):肌动蛋白定位于常染色质与浓缩染色质(C)的交界处(红色突出显示密集标记区);D 图:两种细胞的核仁纤维中心(fc)均检测到肌动蛋白;E 图(大鼠嗜铬细胞瘤 PC12 细胞):过表达 NLS-G15S – 肌动蛋白诱导形成的直肌动蛋白纤维束(箭头);F 图(E 图框选区域高倍):肌动蛋白纤维束及免疫金标记(箭头)。核内肌动蛋白主要以单体形式存在,参与转录、染色质重塑等过程,热休克或血清刺激后可形成纤维。标记:OM(核外膜);NE(核膜)。放大倍数:A 图 ×70,000;B、C 图 ×11,000;D 图 ×80,000;E 图 ×18,000;F 图 ×29,000
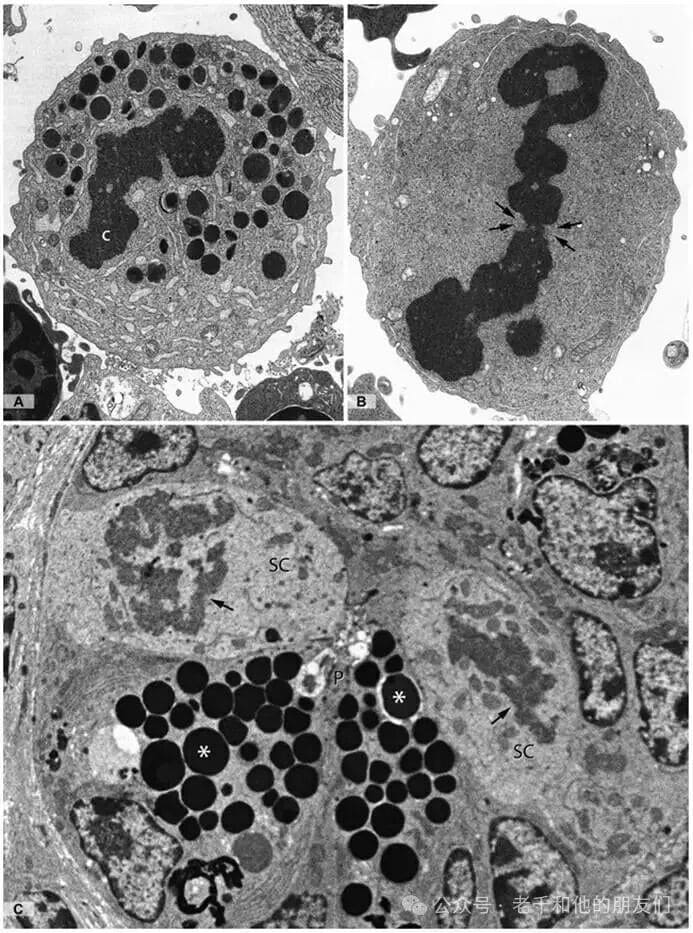
图 10 有丝分裂与细胞分裂的超微结构
细胞分裂由 G2 期结束时的有丝分裂周期蛋白 – Cdc2 复合物触发,目的是将基因组均等分配给子细胞,分前期、中期、后期、末期,随后发生胞质分裂。S 期 DNA 复制后,染色体含两条姐妹染色单体(通过着丝粒连接),依赖粘连蛋白(保证双向定位)和浓缩蛋白(促进染色质浓缩);中心体复制后向两极移动,形成纺锤体(微管 + 相关蛋白),前期核膜解体后纺锤体微管插入染色体动粒,中期染色体排列于赤道板。
A 图(人类骨髓嗜酸性中幼粒细胞)、B 图(有丝分裂原红细胞):均处于中期,可见均匀致密的染色质(C),B 图箭头示染色体着丝粒区域(主缢痕),间期核仁及功能结构域消失,核质与细胞质混合;C 图(小肠隐窝底部):干细胞微环境中,潘氏细胞(P,星号标记巨大分泌颗粒)为干细胞(SC)提供调控信号,两个处于有丝分裂状态的干细胞(箭头示致密染色质)与潘氏细胞紧密接触。放大倍数:A 图 ×10,300;B 图 ×13,500;C 图 ×14,000

图 11 细胞凋亡的典型形态特征(丹参酮 IIA 诱导 KBM-5 细胞)
细胞凋亡是基因控制的生理性程序性细胞死亡,由死亡受体通路或线粒体通路启动,激活胱天蛋白酶,引发特征性形态变化:细胞圆缩、微绒毛消失、质膜完整、染色质高度浓缩并分离(常呈新月形)、核断裂形成核碎片(NB),最终被周围细胞吞噬(凋亡异常可致疾病)。
图 A-E 为丹参酮 IIA 诱导的 KBM-5 人慢性粒细胞白血病细胞凋亡过程:A 图左侧为非凋亡细胞(核与细胞质无变化,箭头示细胞表面微绒毛),右侧凋亡细胞染色质沿核周塌陷呈新月形;B 图(插图为高倍)、C 图:凋亡细胞含完整核膜,染色质浓缩,可见核碎片;D 图(C 图星号标记区域细节):清晰显示完整核膜;E 图(晚期凋亡):细胞含多个核碎片,细胞质严重空泡化。凋亡(I 型程序性细胞死亡)与自噬(II 型)存在功能关联,失衡会引发病理后果。标记:Nucleus(细胞核);M(线粒体);ER(内质网);NB(核碎片)。放大倍数:A 图 ×5,000;B 图 ×4,000;B 图插图 ×9,500;C 图 ×6,500;D 图 ×14,500;E 图 ×3,700
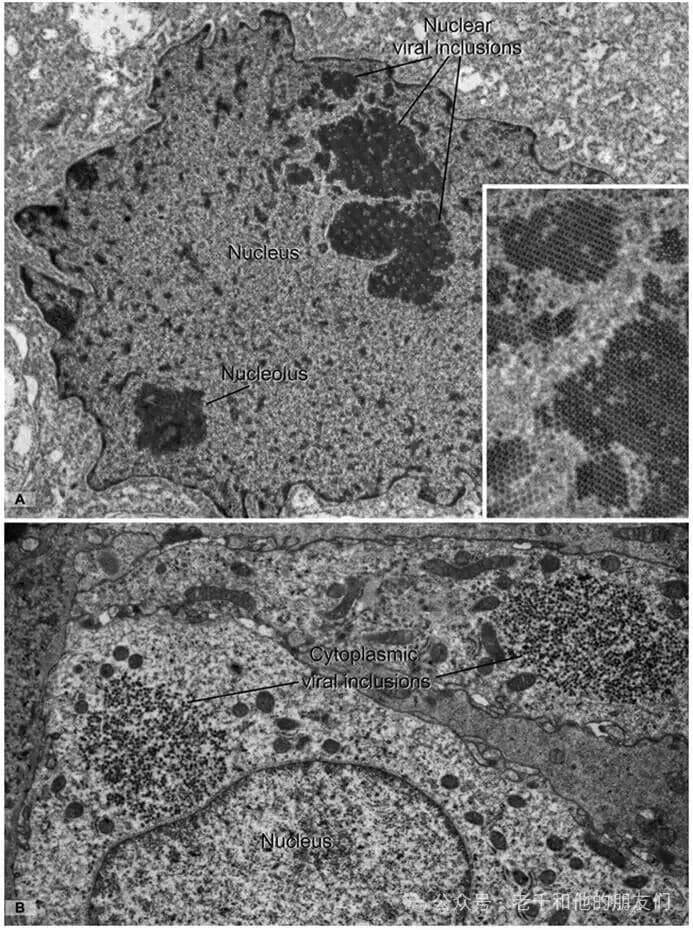
图 12 病毒包涵体的超微结构(多瘤病毒感染)
病毒颗粒体积小(20-300nm),需电子显微镜检测,部分病毒感染后可在细胞内形成聚集体(病毒包涵体)。
样本为肾移植患者肾活检组织(肾小管细胞多瘤病毒感染):A 图(核内)、B 图(胞质内):病毒包涵体由 30-45nm 的球形病毒颗粒组成,呈特征性类晶体排列(A 图插图高倍清晰显示),核内包涵体可与核仁明确区分(结构差异显著)。此外,巨细胞病毒(疱疹病毒科)可引起核质联合包涵体,常见于免疫抑制人群(移植受者、艾滋病患者)。放大倍数:A、B 图 ×12,000;A 图插图 ×35,000
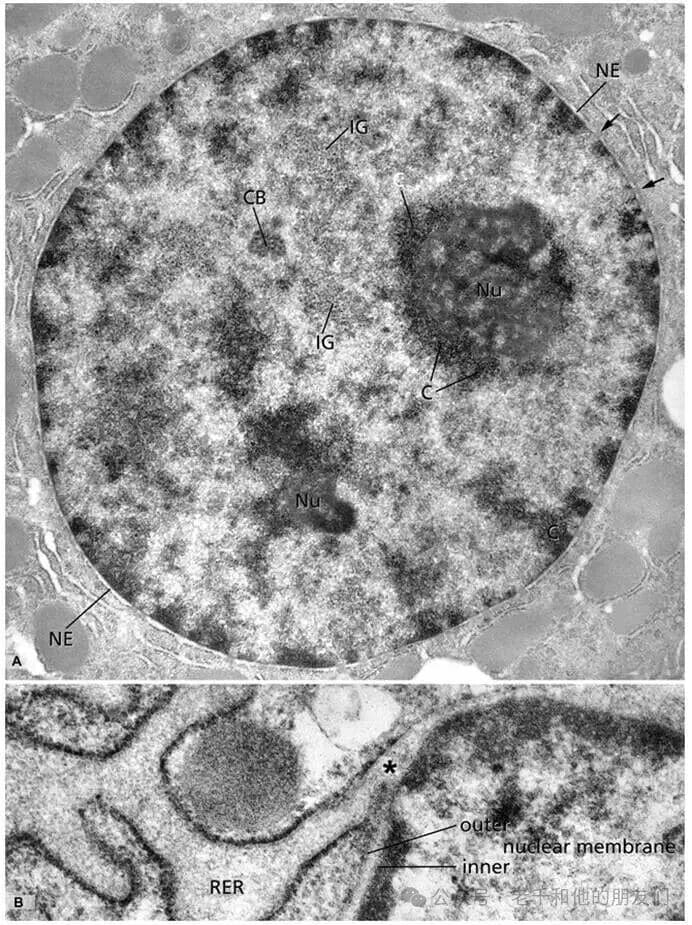
图 13 细胞核的超微结构
细胞核是细胞中最大的细胞器,容纳细胞大部分基因组及基因组织与表达相关的多种分子机制。
图中展示细胞核的核心结构:A 图(核整体结构):核膜(NE)将核质与细胞质分隔,核膜上镶嵌核孔(箭头,为核质间物质交换通道),核内可见染色质间颗粒簇(IG)、卡哈尔体(CB);B 图(核膜细节):核外膜与核内膜围成核周间隙,部分位点核外膜与粗面内质网(RER)膜连通,核周间隙也随之与粗面内质网腔相通(星号标记处)。细胞核内部分为染色体结构域和染色质间空间:浓缩的染色质(异染色质,C)因染色程度高清晰可见,主要分布在核外周(与核纤层附着相关),解聚的常染色质纤维难以分辨;染色质间空间中存在多个功能结构域,其中核仁(Nu)是最显著的结构;染色质间颗粒簇(IG)是剪接因子区室,富含 mRNA 剪接相关的 RNA、蛋白质因子及转录因子等,是剪接复合体的储存 / 组装位点;卡哈尔体(CB,卷曲小体)是研究透彻的小型核结构,暂存转录和 RNA 加工机制的组分。染色质及染色质间结构域的蛋白会与核质持续进行物质交换。
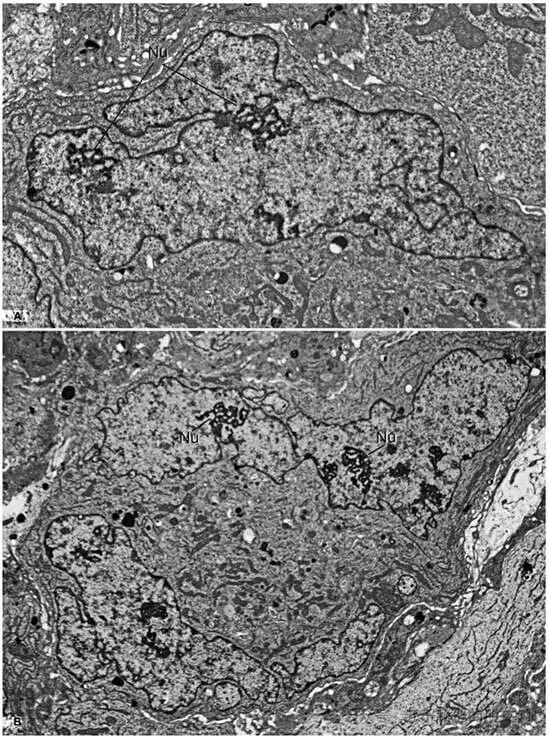
图 14 细胞核形状与大小的动态变化(正常与病理状态)
间期细胞核的形状和大小随细胞类型、细胞活性变化:核形状及功能依赖核纤层蛋白和微管,核大小主要与核质比相关,基因组大小也可能是关键因素。正常细胞中,肝细胞的核大而圆,肠吸收细胞的核呈椭圆形,杯状细胞、内皮细胞、白色脂肪细胞的核极度扁平;圆形的中性粒细胞、嗜碱性粒细胞具有分叶核,且二者穿越毛细血管时核形状可发生可逆变化。
病理状态下(如核纤层蛋白病、癌症),核形状、大小及结构常出现异常,其中核结构(尤其是染色质)异常与基因表达改变相关,是组织病理学诊断的重要依据。图 A、B 为高度恶性人类树突状细胞瘤细胞的核变化:A 图(大分叶核肿瘤细胞):核直径超 20μm,核体积增大导致核质比失衡,核内有增大的核仁(Nu),核仁内可见核仁网(详见图 8),浓缩染色质(异染色质,C)分散分布;B 图(双核肿瘤细胞):两个大核(直径超 30μm)均呈分叶状,内含多个增大的核仁(Nu),核仁内可见核仁网,浓缩染色质分散且存在粗大致密的异染色质聚集体,符合癌细胞核的典型特征。


