作者:孙千 本文转载自公众号:老千和他的朋友们。原文地址:https://mp.weixin.qq.com/s/LuG8dimRVGQiAsjrxwWSmQ
超高分辨率显微镜技术的飞速发展,为生命科学研究提供了前所未有的观测工具,让科研人员能以纳米级精度看透细胞内部的精细结构和动态变化。
Louisa Mezache 等人聚焦当前主流商业超高分辨率显微镜的最新技术突破,系统梳理了共聚焦激光扫描显微镜、结构光照明显微镜(SIM)、受激发射损耗显微镜(STED)、单分子定位显微镜(SMLM)及混合技术的创新成果,为相关领域科研人员提供了全面的仪器选型与应用参考。

共聚焦激光扫描显微镜:经典技术的革新升级
尽管专用超高分辨率技术不断涌现,但共聚焦激光扫描显微镜凭借操作简便、成像质量稳定的优势,仍是科研中应用最广泛的设备之一。近年来,该技术通过融合像素重分配等创新策略,成功突破了传统显微镜的 “衍射极限”(即观测瓶颈),实现了亚衍射分辨率成像。
Confocal.NL推出的 GAIA 显微镜,基于点重扫技术(REscan Technology),巧妙平衡了分辨率与光毒性。其核心原理是对样本进行两次同步扫描:第一次按传统共聚焦模式扫描,用针孔过滤掉模糊的离焦光;第二次把清晰的发射光重新投射到高灵敏度的科学互补金属氧化物半导体(sCMOS)相机上,确保光信号的扩散形态(PSF)与相机像素精准对齐(图 1 为 GAIA 点重扫技术示意图)。
这种设计允许使用更宽的针孔(1.5 艾里单位 / Airy Units)收集更多光子,使原始图像分辨率达到 170 纳米,经消除模糊的去卷积处理后,分辨率更是提升至 120 纳米(相当于能看清细胞内微小颗粒的细节),同时激光功率可低至纳瓦级,大幅降低了对样本的光损伤。
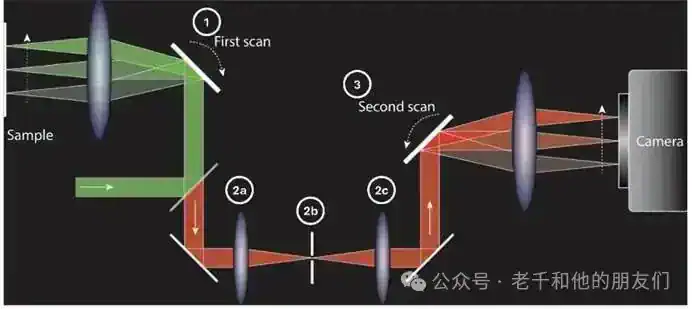
图 1:Confocal.NL公司 GAIA 点重扫描技术示意图。(1)通过高精度反射镜,按传统点扫描显微镜方式对样品进行扫描;(2)样品发射的光经一系列透镜(2a、2c)放大后,通过针孔(2b)滤除离焦光;(3)借助与第一个反射镜同步的第二个反射镜,将清晰信号重新投射到相机上。
GAIA 配备的电动可切换针孔,能适配 30× 至 100× 的各类物镜,支持在小于 500 微米的深度下进行大视野成像(40× 物镜下视野范围达 330×330 微米,图 2 为 GAIA 的电动可切换针孔示意图及针孔尺寸图表),已成功应用于斑马鱼幼虫深层组织成像、细菌孢子休眠与萌发过程的活体观察等研究。
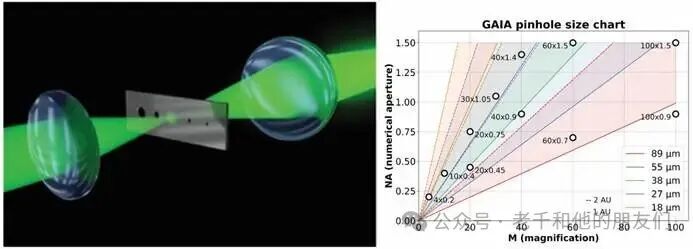
图 2:Confocal.NL公司 GAIA 的可切换针孔。左图:电动可切换针孔示意图,提供多种尺寸选项,可适配各类物镜以维持共聚焦特性;右图:针孔尺寸图表,为优化成像效果提供精准的针孔直径设置参考。
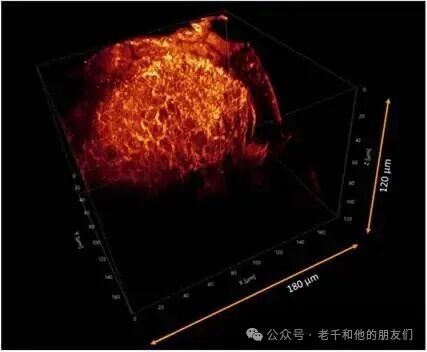
图 3:Confocal.NL公司 GAIA 对厚样本的成像效果。斑马鱼胚胎视顶盖(60 倍物镜,数值孔径 1.3),成像深度约 120 微米,仍能清晰呈现组织细节。
尼康在 AX/AX R 共聚焦显微镜系列中集成的 NSPARC 探测器,采用图像扫描显微镜(ISM)技术与 25 元素单光子雪崩探测器(SPAD)阵列,彻底改变了传统共聚焦的探测模式。
与单一探测器不同,NSPARC 的 5×5 矩阵阵列可捕捉不同方向的横向光信号扩散形态(PSF),每个阵列元素相当于 0.2 艾里单位(AU)的针孔,通过叠加 25 个像素的信号,在保持 1 AU 亮度的同时将分辨率提升至 0.2 AU,结合 Richardson–Lucy 去卷积算法(消除图像模糊的核心算法),可实现 100 纳米的超高分辨率(图 4 为 NSPARC 探测器结构及成像效果对比图)。
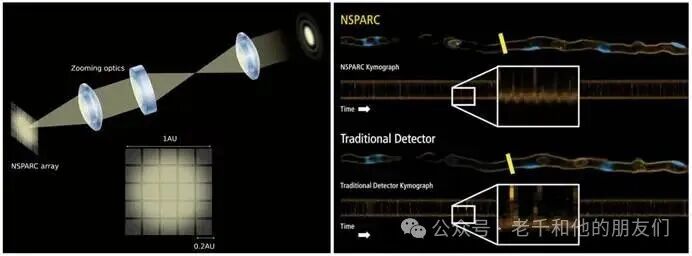
图 4:NSPARC 探测器示意图与成像效果对比。左图:25 元件阵列探测器,每个元件对应 0.2 艾里单位(AU)的针孔,变焦光学系统可将完整的点扩散函数(PSF)精准投射到探测器上;右图:NSPARC 探测器(上图)与传统 GaAsP 探测器(下图)对斑马鱼脉管系统的延时成像对比,放大插图的时间轨迹图显示,NSPARC 能更清晰地呈现血管内皮位置的动态变化。
该探测器具备高灵敏度与低噪声特性,搭配高速共振扫描器,能以 2048×2048 像素分辨率进行动态活细胞成像。其 25 毫米对角线的大视野设计,支持转移性癌细胞迁移、果蝇全脑等大样本的高效成像(图 5 为 NSPARC 成像的细胞与神经元结构示意图),能清晰区分突触前膜和突触后膜等精细结构。
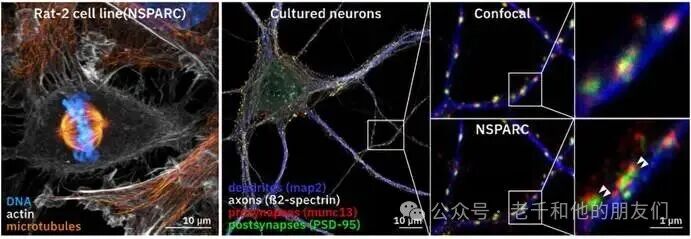
图 5:NSPARC 探测器的成像效果。左图:经 DNA(蓝色)、肌动蛋白(灰色)和微管(橙色)染色的 Rat-2 细胞,经 NSPARC 模块成像并去卷积处理后,清晰展示细胞内核心结构分布;右图:培养的大鼠海马神经元(经树突 map2、轴突 β2 – 血影蛋白、突触前膜 munc13、突触后膜 PSD-95 染色),传统共聚焦图像(上图)与 NSPARC 去卷积图像(下图)对比,NSPARC 能清晰区分突触前膜(红色)与突触后膜(绿色,双箭头所示)。
结构光照明显微镜:计算增强与硬件优化的协同突破
结构光照明显微镜(SIM)的核心原理的是通过带图案的照明光产生莫尔条纹,把样本中的细微空间信息 “编码” 进去,经软件计算分析后,可实现两倍于衍射极限的分辨率。近年来,通过图像重建算法的创新与硬件系统的优化,商业 SIM 仪器已能实现亚 100 纳米分辨率(即能看清小于 100 纳米的细微结构,相当于头发丝直径的千分之一),同时降低了光毒性与操作复杂度。
CSR Biotech 的 MI-SIM 显微镜,创新性地融合了黑塞矩阵解卷积(Hessian-SIM)与稀疏解卷积两种算法,有效解决了 SIM 图像重建中的噪声与模糊问题。Hessian-SIM 利用生物过程的时空连续性增强图像边缘与精细结构,稀疏解卷积则通过约束条件缩小光信号扩散范围(PSF),两者结合使横向分辨率降至 60 纳米,且显著减少成像伪影(即假细节)。
硬件方面,MI-SIM 配备铁电液晶空间光调制器(SLM)、定制拼接偏振旋转器与滨松 ORCA-Flash4.0 V2 sCMOS 相机,支持全内反射荧光(TIRF)、2D/3D SIM 等多种成像模式(图 6 为 MI-SIM 硬件结构示意图)。

图 6:CSR 生物技术公司 MI-SIM 硬件结构示意图。核心组件包括高动态空间光调制器(SLM)、定制拼接偏振旋转器(可实时偏转光偏振方向,实现成像模式高速切换)、滨松 ORCA-Flash4.0 V2 sCMOS 相机,以及自主研发的 ZYNQ-based 高速控制系统(RCM),可在快速切换视野与焦点时实现实时可视化;仪器支持尼康 Ti2-E 或 Evident IX83 平台,操作一键可达,支持序列 / 同步多通道成像,无荧光串扰。
其内置的智能活细胞追踪系统(TRACKER)可自动校正轴向失焦与横向偏移,支持长达 12 小时的长时程成像,已成功应用于线粒体形态观察、HeLa 细胞内囊泡空间分布分析、秀丽隐杆线虫细胞膜修复机制研究等领域(图 7)。
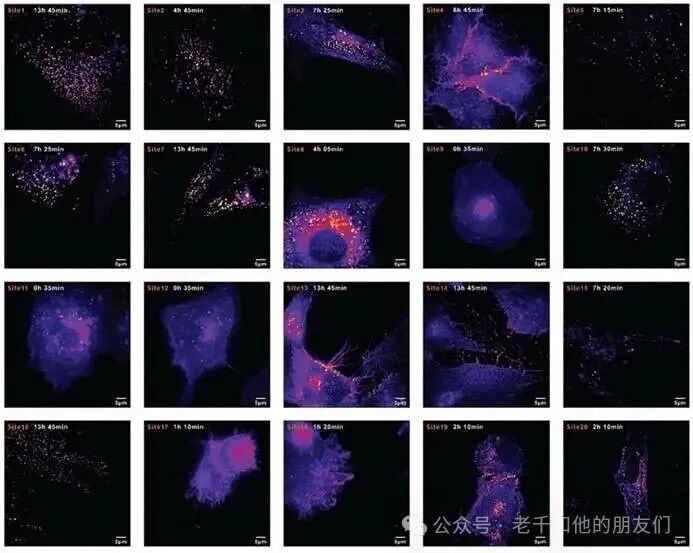
图 7:CSR 生物技术公司 MI-SIM 的 TRACKER 技术成像结果。骨髓干细胞在多视野下迁移的长时程活细胞成像,清晰记录了 20 个感兴趣区域 20 小时的细胞迁移轨迹(比例尺 5 微米)。
蔡司的 Lattice SIM 5 采用 3D 晶格光斑照明模式,通过光栅衍射使五种级次的光进入物镜并产生 13 种相位,同时在多个方向和角度调制光线,仅需横向移动晶格图案即可一次性捕捉全方向莫尔条纹(2D 成像需 9 幅图,3D 成像需 13 幅图),大幅减少样本的照明剂量,降低光损伤。
该仪器配备五种适配不同激光波长的晶格光栅频率,以及适用于 10× 至 40× 物镜的通用 ApoTome 光栅,支持 Leap 模式与 Burst 模式:Leap 模式通过间隔采集 z-stack 切片并计算补全数据,平衡成像速度与光毒性;Burst 模式则以高达 255 帧 / 秒(fps)的帧率实现高速 3D 成像,有效减少运动模糊。
结合基于 Richardson–Lucy 算法的 SIM² 解卷积技术,Lattice SIM 5 可实现亚 100 纳米分辨率,且能实时适配不同成像条件,已成功应用于 HeLa M 细胞的膜蛋白转运追踪、轴突力学响应分析等研究。
受激发射损耗显微镜:低光毒性与高分辨率的精准平衡
STED 显微镜的核心原理是通过环形损耗光束选择性 “熄灭” 荧光,只让焦点中心纳米级区域的荧光发光,从而将照明区域精准限制在极小范围,可实现数十纳米的空间分辨率。针对传统 STED 技术光毒性强、操作复杂等问题,商业仪器厂商通过光束整形、荧光寿命分析等创新,显著提升了技术的实用性与适用性。
徕卡的 STELLARIS STED 系统,将纳米成像能力与 STELLARIS 共聚焦平台相结合,具备出色的光谱灵活性与探测灵敏度。该系统配备脉冲白光激光(440-790 nm)与三种 STED 激光(脉冲 589 nm、连续波 660 nm、脉冲 775 nm),搭配 Power HyD 系列探测器 ——Power HyD S 优化蓝绿光谱探测,Power HyD R 支持高达 850 nm 的红外光谱探测,且均兼容荧光寿命成像(FLIM)、荧光相关光谱(FCS)等技术。
其核心创新 TauSTED 技术,融合 STED 信息与荧光寿命数据,利用有效光信号扩散形态(PSF)中心与边缘光子的寿命差异增强分辨率,在低于 1% 的 STED 光剂量下,就能将分辨率从共聚焦的 250 纳米提升至 150 纳米(图 8 为 STED 与荧光寿命读取示意图)。
最新升级的 TauSTED Xtend 技术,通过提取有效 STED PSF 的光物理特征,结合加速 Richardson–Lucy 算法,在相同激光功率下将分辨率进一步提升至 75 纳米(图 9 为 TauSTED 与 TauSTED Xtend 的分辨率对比图)。该系统已广泛应用于神经元铁稳态研究、隧道纳米管内肌动蛋白细胞骨架与线粒体动态观察、基因组组织分析等领域。
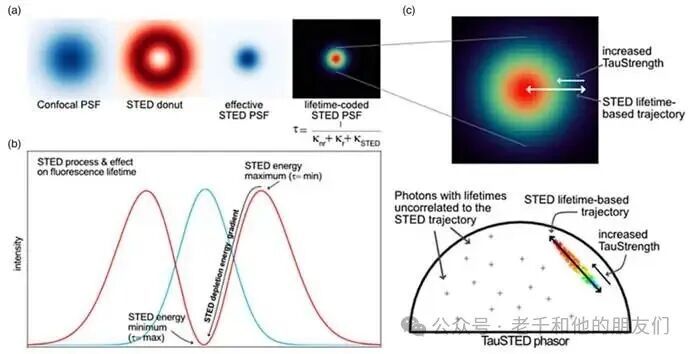
图 8:STED 技术与荧光寿命读取原理示意图。(a)共聚焦、STED 环形光束、有效 STED 点扩散函数(PSF)及寿命编码 STED PSF 的结构示意;(b)STED 作用过程及其产生的荧光寿命梯度;(c)TauSTED 技术原理示意图,蓝色代表较短荧光寿命,红色代表较长荧光寿命。
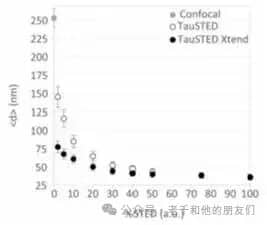
图 9:徕卡 TauSTED 与 TauSTED Xtend 分辨率对比图。共聚焦、TauSTED 与 TauSTED Xtend 技术的分辨率对比:低 STED 激光功率(<1%)下,TauSTED 可将分辨率从共聚焦的 250 nm 提升至 150 nm;相同功率下,TauSTED Xtend 进一步将分辨率提升至 75 nm。
abberior Instruments 推出了 FACILITY、STEDYCON、INFINITY 三大系列 STED 仪器,满足不同用户的个性化需求。FACILITY 系列配备两种脉冲损耗激光(595 nm、775 nm)与五种脉冲激发激光(405 nm、488 nm、518 nm、561 nm、640 nm),结合 RAINBOW 光谱探测(1 nm 精度)与 TIMEBOW 寿命成像技术,可灵活适配各类实验需求。
其 EASY3D 光束整形技术通过空间光调制器(SLM)生成承载 XY-STED 与 Z-STED 的单一光束,可在 20 纳米横向分辨率与 75 纳米 3D 等轴分辨率之间灵活调节(图 10 为 abberior 的 STED 光束整形技术示意图)。
为解决厚样本成像中的像差问题(即光线畸变导致的模糊),FACILITY 集成 RAYSHAPE 自适应光学系统,通过 140 个驱动器的可变形反射镜动态校正样本引起的光束畸变,在接近物镜工作距离的深度下仍能保持高分辨率(图 11 为RAYSHAPE 技术实现果蝇胚胎深层组织成像的效果对比,70 微米深度下仍能清晰成像);
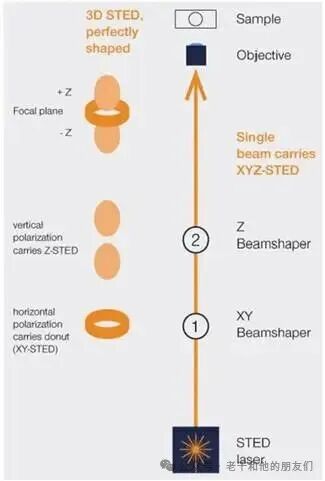
图 10:abberior 的 STED 光束整形技术示意图。二维(XY)与三维(Z)STED 光束由激光光路中的空间光调制器(SLM)生成,通过水平偏振承载 XY-STED 环形光束、垂直偏振承载 Z-STED 光束,实现单一光束同时承载 XY-STED 与 Z-STED 损耗功能。
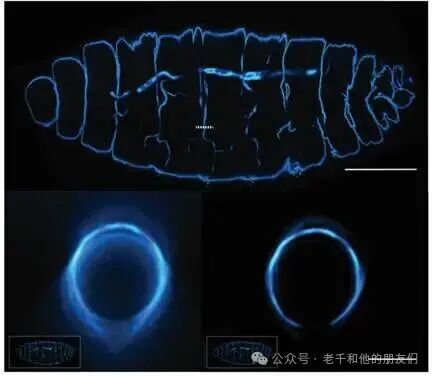
图 11:abberior 的 RAYSHAPE 自适应光学技术成像效果。上图:经 abberior LIVE 610 染色几丁质的 17 期果蝇胚胎深层组织成像,RAYSHAPE 可变形反射镜技术能实现比传统 STED 更深远的成像深度(比例尺 100 微米);下图:上图虚线位置的横截面成像对比,70 微米深度下,使用 RAYSHAPE(右图)比未使用(左图)成像更清晰(比例尺 10 微米)。
MATRIX 23 元素阵列探测器则可直接测量并扣除背景信号,无需复杂后处理。STEDYCON 作为入门级模块,可适配任意宽场显微镜,通过光纤对齐保证激发与损耗光束的稳定叠加,搭配浏览器端简易操作软件,使新手用户也能快速获取超高分辨率图像(图 13 为 abberior STEDYCON 的模块结构示意图)。

图 13:abberior STEDYCON 模块结构示意图。专为显微镜新手设计的入门级 STED 系统,是可适配任意宽场显微镜机身的模块化设备,操作简便易上手。
INFINITY 系列则提供开放式定制平台,支持 375-1320 nm 波长的脉冲或多光子激光配置,可与原子力显微镜(AFM)等技术集成,已应用于果蝇生殖颗粒中 RNA – 蛋白凝聚体的双相组织观察、星形胶质细胞表面拓扑分析等前沿研究(图 12 为 abberior 解卷积技术提升成像质量的效果对比)。
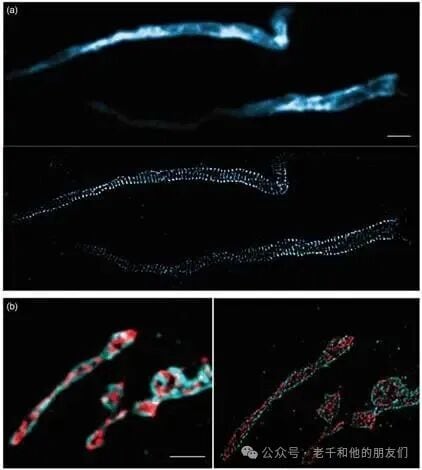
图 12:abberior 新型去卷积技术成像效果对比。(a)经 Alexa 594 标记 βIV – 血影蛋白的小鼠新皮质轴突起始段,未使用(上图)与使用(下图)去卷积技术的成像对比(冷冻切片厚度 20 微米,比例尺 1 微米);(b)经 abberior STAR 580 标记 GM130 蛋白、abberior STAR 635P 标记巨蛋白(Giantin)的高尔基体,未使用(左图)与使用(右图)去卷积技术的成像对比(冷冻切片厚度 20 微米,比例尺 1 微米),使用后可清晰区分细胞内精细结构。
单分子定位显微镜:单分子水平的精准观测
SMLM 技术利用荧光分子 “随机闪烁” 或 “光切换” 的特性,通过反复成像与精确定位,可实现 10-20 纳米的超高分辨率(相当于能看清单个分子的位置),揭示传统显微镜无法观测的亚细胞精细结构。近年来,商业 SMLM 仪器在照明均匀性、3D 成像能力、多色兼容等方面取得显著突破,进一步拓展了应用场景。
Abbelight 的 SAFe MN360 显微镜,基于自适应扫描可调激发区域(ASTER)技术,解决了传统 SMLM 高斯照明导致的视野内激发不均问题(即部分区域荧光强、部分弱)。该技术通过双振镜光栅扫描系统,将小尺寸高斯光束快速扫描整个视野,生成 “平顶” 照明轮廓,确保荧光分子在 150×150 微米(100× 物镜)或 250×250 微米(60× 物镜)的大视野内获得一致的激发条件(图 14 为 Abbelight 的 ASTER 技术示意图)。
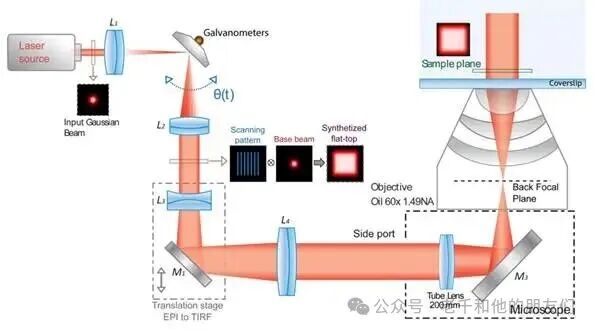
图 14:Abbelight 的 ASTER 技术示意图。通过双振镜光栅扫描系统生成均匀照明场,核心组件包括四个特定焦距的透镜(L1-L4)与介质反射镜(M1);小尺寸高斯输入光束经 L1 与 L2 间扫描形成平顶照明轮廓,再通过全内反射荧光(TIRF)平移台及 L3、L4 放大,在背焦平面聚焦后,于样品处形成平顶激发轮廓(配备 60×1.49NA 油浸物镜)。
SAFe MN360 的双相机光谱解混模块,通过光束分束器与二向色镜将两种远红荧光团的发射光谱分离至不同相机,实时计算光子比率以区分荧光团类型,有效克服多色 SMLM 中的色差与荧光团光物理特性差异问题。
在单通道模式下,该系统通过 50:50 光束分束器分别捕捉无畸变 PSF(用于 XY 方向定位)与像散 PSF(用于 Z 方向探测),结合三次样条(C-spline)插值算法精准建模不同深度的 PSF 形状,显著拓展了 3D 成像的深度范围。该仪器已成功应用于微管修复事件可视化、TRPV2 阳离子通道聚类定量、海马体多突触扣结的 3D 纳米级定位等研究。
布鲁克的 Vutara VXL 显微镜,采用双平面检测技术实现高效 3D 亚衍射分辨率成像。其核心原理是通过 50:50 光束分束器将聚焦光分为两个沿轴分离的光路,利用荧光分子在两个成像平面上的强度差异确定其 z 轴位置,结合荧光微球校准的 3D PSF 拟合,实现精准的三维定位(图 15 为 Bruker 的 Vutara 双平面检测技术示意图;图 16 为双平面检测 z 轴定位原理示意图)。
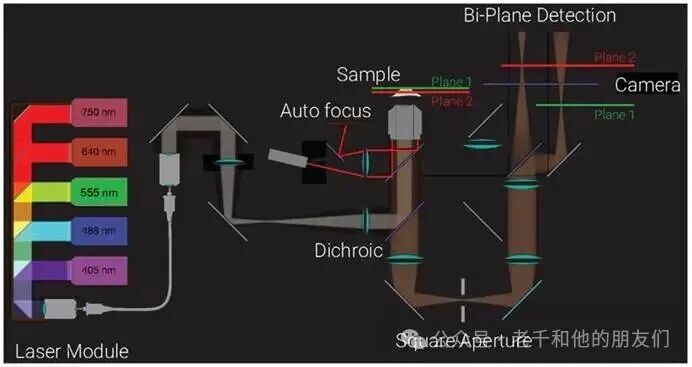
图 15:布鲁克 Vutara 双平面检测技术光束路径示意图。样品发射的荧光经二向色镜分离为两个独立光学平面,分别投射到相机传感器的不同区域(平面 1 与平面 2),支持 405 nm、488 nm、555 nm、640 nm、750 nm 激光波长,具备自动对焦功能。
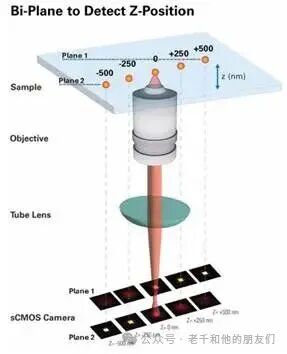
图 16:布鲁克 Vutara 双平面检测 z 轴定位原理示意图。可同时捕获来自两个不同焦平面的荧光发射体信号,每个发射体的点扩散函数(PSF)会在两个相距约 1 微米的成像平面上形成略有差异的图像,通过两个平面间的强度差异,可精准确定每个发射体的 z 轴位置(z 轴范围 – 500 nm 至 + 500 nm)。
Vutara VXL 采用避光封闭设计,配备 60X/1.30NA 硅油物镜与滨松 sCMOS 相机,支持 3 种标配激光(405 nm、555 nm、638 nm)与 2 种可选激光(488 nm、750 nm),可实现多达五种颜色的连续 3D 成像,成像深度可达 50 微米。
通过校准并校正多光谱成像中的焦移与横向位移,该系统有效降低色差影响,且集成自动化微流控单元,支持多路 DNA-PAINT、荧光原位杂交(FISH)、染色质追踪等应用。在科研中,Vutara VXL 已用于染色质纳米结构可视化、病毒粒子定位与复制周期定量等研究。
混合技术:MINFLUX 的跨维度突破
作为首个商业化的混合超高分辨率技术,abberior 的 MINFLUX 融合了 SMLM 与 STED 的核心原理,实现了单纳米级分辨率与低光毒性的完美结合。其创新之处在于采用环形激发光束,将暗中心尽可能靠近目标分子,通过移动光束并测量不同位置的光子通量,迭代优化分子定位精度 —— 当分子位于光束暗中心时,激发强度最弱,光子发射最少,据此可实现超高精度定位(图 17 为 abberior 的 MINFLUX 技术示意图)。
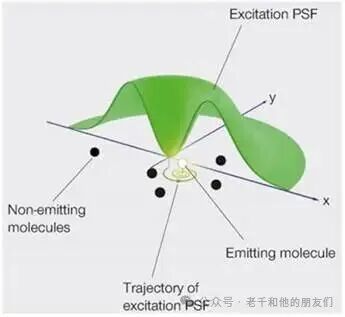
图 17:abberior 的 MINFLUX 技术原理示意图。采用中心强度为零的环形激发光束靶向空间特定区域,通过移动环形光束中心至荧光团附近不同位置,测量各位置的光子发射量,当荧光分子靠近光束零强度中心时发射光子最少,据此实现分子的超高精度定位。
MINFLUX 的 2D 与 3D 激发光束通过反射式 SLM 生成,横向扫描由电光元件介导,轴向扫描采用可变形反射镜,实现微秒级时间分辨率。系统配备亚纳米级压电稳定装置与激光漂移校正模块,有效抵消室温波动、环境振动等外部干扰,支持长时程成像。该技术的分辨率可达单纳米级,且光子消耗极低,大幅减少光漂白与光毒性,适用于活细胞动态事件追踪与固定样本的单分子结构分析。
目前,MINFLUX 已成功应用于视网膜光感受器突触活性区的 3D 成像、驱动蛋白 – 1 运动轨迹的实时追踪、PIEZO1 离子通道构象变化的动态观测等前沿研究,为分子生物学机制解析提供了全新视角。
技术趋势与未来挑战
当前商业超高分辨率显微镜的技术创新呈现三大核心趋势:分辨率持续向单纳米级突破,光毒性通过低功率激光、自适应照明等技术显著降低,成像能力向大视野、深层组织、长时程方向拓展。同时,仪器易用性的提升成为普及关键 —— 模块化设计(如 STEDYCON)、AI 辅助参数设置(如蔡司 ZEN 软件)、远程操作功能等,使非专业用户也能开展超高分辨率成像研究。
然而,该领域仍面临诸多挑战:超高分辨率成像产生的海量数据对存储与处理能力提出更高要求;复杂样本成像中的伪影控制需要进一步优化;高端仪器的高成本与普及性之间的平衡仍是行业亟待解决的问题。
未来,随着数据处理算法的革新、新型荧光探针的开发以及多模态技术的融合,超高分辨率显微镜将在生命科学研究中发挥更重要的作用,持续推动对细胞结构与功能的深度探索。
参考资料Advancing Super-Resolution Microscopy: Recent Innovations in Commercial Instruments


